什么是温度?
构成物质的微观粒子(分子,原子,电子)在永不停息的做无规则运动
宏观下,温度表示物体的冷热程度;缩小到原子层面上,温度反应微观粒子的运动剧烈程度。

根据热学第二定律 “克劳修斯的表述为 热量可以自发的从温度高的物体传递到温度低的物体,但不可能自发的从温度低的物体传输到温度高的物体。”
因此,导致热量在物体间传递的方式有3种:
- 热传导 (固体之间热量传递)
- 热对流 (液体通过内部运动,得到热量均衡)
- 热辐射 (热源以电磁波等辐射形式发散热能)
在质量不变的前提下,温度越高的物体内能越大。所以以上三种方法都会导致物体内能改变。但是,还有另一种方法能导致物体内能改变——物质状态变化。(0度的水比0度的冰具有更高的内能)
常见物质状态包括:固体,液体,气体。同种物质,相同质量下,气体内能大于液体内能大于固体内能。换言之,气体分子的运动剧烈程度远远高于同种液体和固体分子。
分子运动越剧烈,物质整体对个体分子的约束力越弱,因此体积越大。质量不变的情况下,固体密度大于液体和气体密度。
这是一个常用规律,对绝大多数物质都适用,但是化学中总有“例外”
第一个例外——结构变化
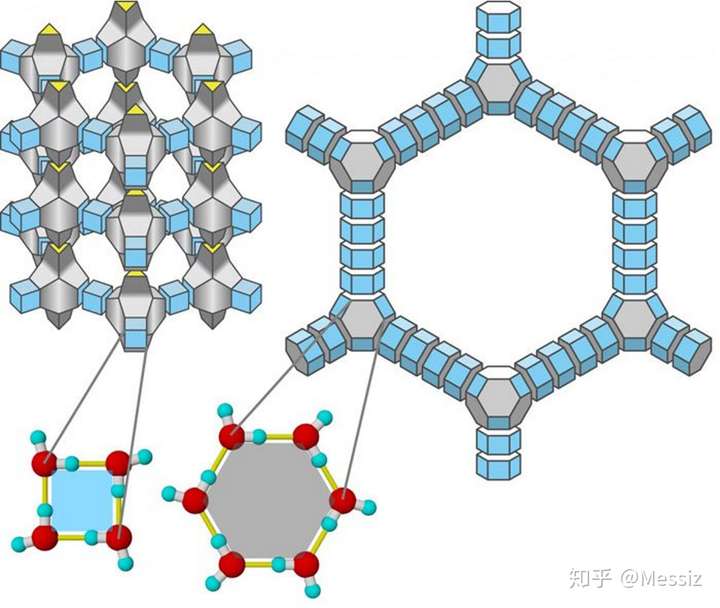
【左图】水液态分子结构,【右图】冰固态分子结构。
液态水为V形分子,分子间有偶极作用,特殊结构是氢键,分子间距离均等,构成液态整体。
但是,当温度降低到0度时,一标准大气压下水的分子结构发生改变。它不再是V形分子,固态冰为六角形水晶结构。

水变成冰时,原子结构改变,分子间距加大,结构紧密的许多个分子拼凑出一片“冰晶”
因此,水的密度997m/kg, 冰密度 934m/kg, 冰的密度略小于水的密度。
总结——同种质量下固体密度大于液体和气体密度。若物态变化时微观粒子结构变化,结果另当别论。
第二个例外——压强
二氧化碳的固态“干冰”,由于制冷功能优越,常用与机械制造和化学工程上。但是,地球上不存在自然的液态二氧化碳。
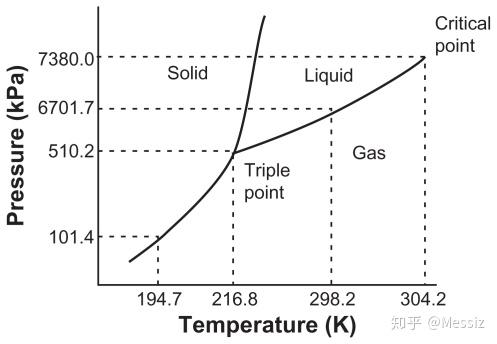
CO2三相点——由于地球上的气压太小,无法将二氧化碳压缩至液态。当气体达到凝固点时,直接凝华为固体。
总结——讨论物质状态和物质密度时,必须考虑压强。
你可以看看这个网址:
https://www.zhihu.com/question/65161522
希望这对你有所帮助,能帮助到你是对我最大的快乐 (๑•̀ㅁ•́ฅ✧